업무안내
[호주-뉴질랜드] 식품 기준청, 영아용 조제분유 표준 승인
- 작성일2024/07/04 15:18
- 조회 232
영아용 조제분유에 대한 분류 기준 재정의 및 요구 사항 수정
2024년 6월 4일, 호주-뉴질랜드 식품기준청(FSANZ)은 영아용 조제분유 표준(P1028)의 승인하고 이를 식품과 식량 문제를 담당하는 호주 및 뉴질랜드 장관으로 구성된 식품장관회의(FMM)에 통보함. FMM은 식품기준청이 통보한 표준의 검토 여부를 60일 이내에 결정해야 하며, 별도의 검토 요청이 없을 경우 해당 표준은 5년의 전환 기간을 거쳐 발효될 예정임
1. 배경
호주-뉴질랜드 식품기준청은 영아용 조제분유 표준(P1028)의 개정을 통해 분유를 섭취하는 영아의 안전을 보장하고, 보호자가 제품을 안전하게 이용할 수 있도록 함. 개정은 영아용 조제분유(생후~6개월 미만), 영아용 후속 조제분유(생후 6~12개월) 및 영아용 특수 의료 목적의 조제분유(SMPPi)를 대상으로 함. 주요 수정사항은 제품 라벨링 및 포장 요구 사항, 영양 정보 보강과, 특수 의료 목적 제품에 대한 판매 제한 등이 있음
* 특정 영양소의 섭취, 대사 등의 능력이 손상된 유아의 식이 관리를 위해 특별히 제조된 제품으로, 의료 감독 하에 사용되며 의학적으로 진단된 영아의 질병, 장애 등의 상황을 위한 식이 관리 제품
* 특수 식이용 영아용 조제식 제품(IFPSDU) 의 범주명을 영아용 특수 의료 목적 제품(SMPPi)으로 변경
2. 주요 내용
1) 제한 추가 및 추가 요구 사항 (표준 2.9.1 수정 사항)
- 영아용 조제분유와 영아용 후속 조제분유의 불소 함량은 17μg/100kJ을 초과해서는 안됨
- 영아용 조제분유 및 영아용 후속 조제분유에는 과당 및 자당(설탕)이 첨가되어서는 안됨 (단, ① 부분 가수분해 단백질로 제조된 경우, 과당 및 자당(설탕)이 탄수화물 원료로 첨가될 수 있으며, ② 과당 및 자당(설탕)이 조제분유에 포함된 탄수화물의 20%를 초과하지 않는 경우에도 첨가하는 것이 허용됨)
- 영아용 조제분유 및 영아용 후속 조제분유의 구성 요건을 차별화하여, 단백질 최소량, 비타민 D 최대량, 칼슘 최대량, 철 최소량, 콜린 최소량, 이노시톨 최소량 및 L-카르니틴 최대량 등을 규정함
2) 영아용 조제분유 및 영아용 후속 조제분유 제품 표준
- 영양 성분 기준
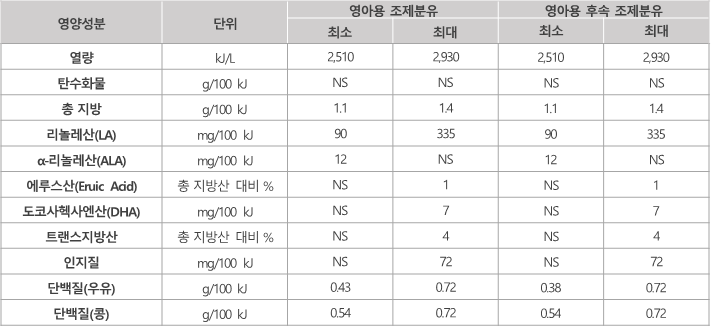
- 라벨링 및 포장 요구 사항
- 영아용 조제분유와 영아용 후속 조제분유를 텍스트, 그림 또는 색상을 사용하여 다른 식품과 구별하도록 함
- 단백질 공급원(소 우유, 염소 우유, 양 우유 등)을 포장 전면에 기재해야 함
- 추가된 비타민과 미네랄은 성분 표기 시 모든 성분을 각각 ‘비타민’과 ‘미네랄‘이라는 소제목 아래 나열하되, 중량 순으로 나열하지 않아도 됨
- 부분적으로 가수분해된 제품의 경우, 단백질 공급원 표기 바로 옆에 해당 문구 또는 유사한 의미를 가진 단어를 기재해야 함
- 분말, 농축 및 바로 마실 수 있는 제품에 대한 ‘지침을 정확히 따르십시오’ 경고 문구를 모든 제품 유형에 적용되는 단일 경고 문구로 단일화 함
- 영아용 조제분유와 영아용 후속 조제분유의 라벨에 저유당 및 유당 무첨가 표현을 금지함
- 알레르기 유발 물질 및 잠재적 알레르기 유발 물질에 대한 요구 사항을 강화함
3) 영아용 특수 의료 목적 제품 표준
- 판매 제한 사항
- 영아용 특수 의료 목적 제품의 판매를 의료 전문가, 영양사, 의료 기관, 약국, 책임 기관, 또는 해당 제품의 주요 판매자로 제한함